基因编辑的时代已经到来!华人科学家重排原子精准编辑基因
编者按:本文来自微信公众号“学术经纬”,原题目“华人科学家化身生命炼金术师,重排原子精准编辑基因”,36氪经授权发布。
当我们在谈论生命时,我们谈论的都是化学分子。DNA也好,蛋白质也罢,正是这些生物大分子发生的原子重排,才催生出无数生化反应,为地球带来生命。
本研究的主要负责人David Liu教授(图片来源:Broad研究所)
今日,Broad研究所的华人学者David Liu教授公布了一项了不起的研究!他的团队开发了一种“碱基编辑器”,能在细胞内用简单的化学反应,使DNA的一种碱基进行原子重排,让它变成另一种碱基。与CRISPR-Cas9等流行的基因编辑手段不同,这种技术无需使DNA断裂,就能完成基因的精准编辑。这项研究发表在了顶尖学术期刊《自然》上。
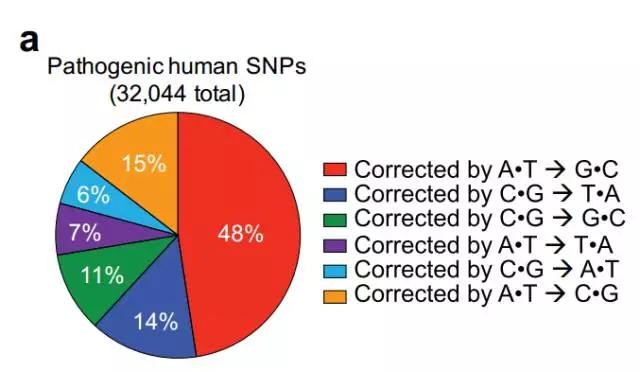
将近一半的致病变异来源于C-G组合到A-T组合的改变(图片来源:《自然》)
要看懂这项研究,我们先来看看DNA本身。我们知道,DNA的双螺旋结构由4种碱基:腺嘌呤(A)、胸腺嘧啶(T)、胞嘧啶(C)与鸟嘌呤(G)组成。它们A和T配对,C和G配对,就像字母一样,编写了人类的遗传信息。然而由于化学结构的问题,C这个字母不大稳定,容易出现自发的脱氨突变,把原本的好好的C-G组合,变成A-T组合。据估计,每天人类的每个细胞里都会出现100-500次这样的突变。而人类已知的致病单碱基变异,高达一半属于这种突变。
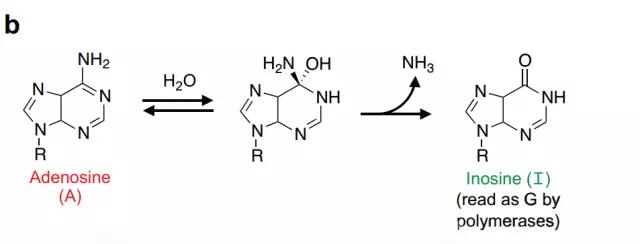
合适的脱氨反应能将腺嘌呤转变为结构类似于鸟嘌呤的肌苷(图片来源:《自然》)
换句话说,如果我们能定点修复这些基因突变,把A-T变回C-G,就有望从根源上纠正人类的许多遗传疾病。这正是Liu教授团队的研究思路。在实验室中,他们观察到了一个很有意思的现象——腺嘌呤(A)在出现脱氨反应后,会变成一种叫做肌苷的分子,而它与鸟嘌呤(G)的结构非常接近,也能成功骗过细胞里的DNA聚合酶。简单的几轮DNA复制后,A-T组合就能变回C-G。
但科学家们遇到一个棘手的问题——自然界中并没有能够在DNA中催化腺嘌呤进行脱氨反应的酶。
如果没有现成的道路,那就开辟一条!在人体中,科学家们发现了一种叫做TadA的酶,它能催化转运RNA上的腺嘌呤(A),使它脱氨。尽管催化的对象不同,但Liu教授的团队认为它有足够的应用潜力。于是,利用演化的力量,科学家们对TadA进行了改造。他们将编码TadA的基因引入大肠杆菌内,并寄希望于这种酶能在大肠杆菌快速的繁衍中,突变出催化DNA腺嘌呤的能力。
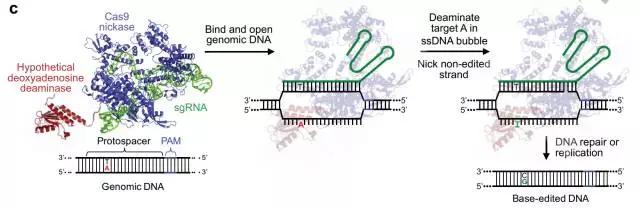
本研究中,碱基编辑器的作用机理(图片来源:《自然》)
同时,科学家们也想到,DNA上的腺嘌呤特别多,总不能把他们全都转化为鸟嘌呤吧。因此,特异性地对某个碱基进行催化,是这套系统迈入实际应用的关键。Liu教授想到了自己的实验室邻居张锋教授,这名华人学者以CRISPR基因编辑技术而闻名于世。如果我们借助CRISPR-Cas9系统的精准,但不让它切开双链DNA,或许就能定点对腺嘌呤进行原子重排,让它变成另一种碱基。为此,科学家们在筛选TadA酶的过程中,也同样引入了一套切不动DNA的特殊CRISPR-Cas9系统,用于精准定位。
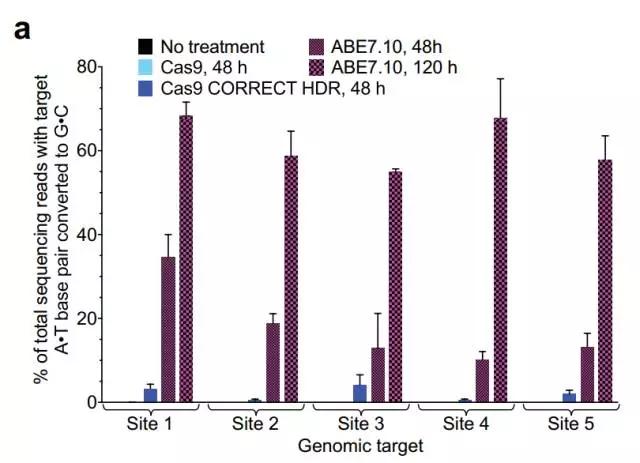
功夫不负有心人!这套系统虽然极为复杂,但在经历了漫长的7代筛选后,Liu教授团队终于开发出了一款全新的“碱基编辑器”,其核心正是能有效针对DNA的TadA酶。无论是在细菌里,还是在人类细胞中,这款编辑器都能顺利发挥作用。在人类细胞里,它的编辑效率超过了50%!
这套系统能有效用于人类细胞(图片来源:《自然》)
尽管这套系统利用了CRISPR-Cas9系统,但科学家们在这篇论文里指出,他们开发的技术与CRISPR-Cas9系统各有千秋。在矫正单碱基突变方面,它比CRISPR-Cas9系统更为有效,也更“干净”。它几乎没有引起任何随机插入和删除等突变,在全基因组里的脱靶效应也要好于CRISPR-Cas9技术。要知道,这可是人们对CRISPR-Cas9技术安全性的最大担忧之一。
先前,研究人员们也同样开发了编辑其他碱基的方法。目前,Liu教授的团队已经有了把C变成T,把A变成G,把T变成C,以及把G变成A的工具。诚然,这些工具目前距离人类临床应用还有不小的距离。但要知道,它只涉及碱基的原子重排,无需让DNA双链断裂,从而降低了基因治疗过程中的风险。此外,许多遗传病都是单基因突变,用这些工具进行治疗也显得更为有的放矢。
我们感谢Liu教授的团队为我们带来如此令人兴奋的基因编辑新工具。毫无疑问,基因编辑的时代已经到来,你准备好迎接冲击了吗?
参考资料:[1] Programmable base editing of A•T to G•C in genomic DNA without DNA cleavage